Resumen
Las QA son lesiones con un potencial variable de transformación maligna, pero con una evolución difícil de predecir. Los métodos de imagen cutánea no invasivos permiten evaluar mejor las lesiones de QA, así como establecer un diagnóstico con mayor especificidad y sensibilidad. Esta revisión es la primera que reúne todos los métodos de imagen cutánea útiles en el diagnóstico y el seguimiento del tratamiento de las QA.
Comentario
La QA o queratosis solar es una lesión precancerosa derivada de los queratinocitos que se encuentra con frecuencia en adultos y que típicamente se desarrolla en partes de la piel expuestas al sol. El campo de cancerización (CC) se refiere a la región anatómica que engloba o se encuentra adyacente a las lesiones de QA dentro de la piel visiblemente dañada por el sol.
Su localización en áreas expuestas a la luz solar (cabeza y cuello), así como la presencia de múltiples lesiones en diferentes etapas (incluidas las subclínicas) en el mismo paciente, dificultan el uso de la biopsia y el examen histopatológico como método de diagnóstico y seguimiento. Como resultado, cada vez es más necesario desarrollar técnicas no invasivas para el diagnóstico, la estadificación y la valoración de la eficacia del tratamiento de estas lesiones. Las técnicas más utilizadas son la dermatoscopia, la ecografía de alta frecuencia, la ecografía de alta frecuencia guiada por dermatoscopia, la tomografía de coherencia óptica (TCO) y la microscopia confocal de reflectancia (MCR).
Queratosis actínica: sistemas de clasificación y aspectos clínicos, histopatológicos y terapéuticos
Aspectos clínicos e histopatológicos
En 1999, Yantsos introdujo una clasificación histológica de las QA según la extensión de las células atípicas dentro de la capa epitelial. Las lesiones histológicas de bajo grado, denominadas KIN1, muestran una distribución de células atípicas confinadas al tercio inferior de la epidermis y se considera que tienen un riesgo mínimo de convertirse en cáncer. Las lesiones clasificadas como KIN2 y KIN3 son de grados histológicos más altos. Muestran células atípicas que se extienden hasta los dos tercios inferiores y a través de todo el grosor de la epidermis, respectivamente, y se asocian con una mayor probabilidad de transformación maligna.
Clínicamente, las lesiones de QA se gradúan según el sistema de Olsen et al., que las clasifica de grado 1 a grado 3. Este sistema tiene limitaciones: estudios recientes indican que los grados clínicos de Olsen subestiman la gravedad histológica en el 62,4 % de los casos.
El sistema de clasificación clinicopatológica propuesto por Rowert-Huber en 2007 se diseñó para destacar que todas las lesiones de QA son CCE in situ desde el inicio, pero en diferentes etapas de progresión. Cuando aparecen múltiples grados dentro de la misma lesión, el grado más alto determina la etapa.
Como no es posible predecir qué lesiones se volverán invasivas, todas las lesiones de QA deberían tratarse.
Otras investigaciones revelan que la QA, incluso en etapas tempranas, tiene el potencial de progresar a CCE cutáneo invasivo sin la necesidad de pasar por etapas intermedias de neoplasia intraepidérmica de queratinocitos. Esto sugiere que debería valorarse el tratamiento de todas las lesiones de QA y el campo de cancerización.
Evaluación no invasiva de la queratosis actínica
Dermatoscopia
Puede amplificar la imagen para observar las estructuras morfológicas en la epidermis y la dermis papilar.
En conjunto, el patrón dermatoscópico de la QA es la apariencia de «fresa», que se caracteriza por una pseudorred roja formada por eritema de fondo interrumpido por aberturas foliculares o anexiales prominentes (figura 1).
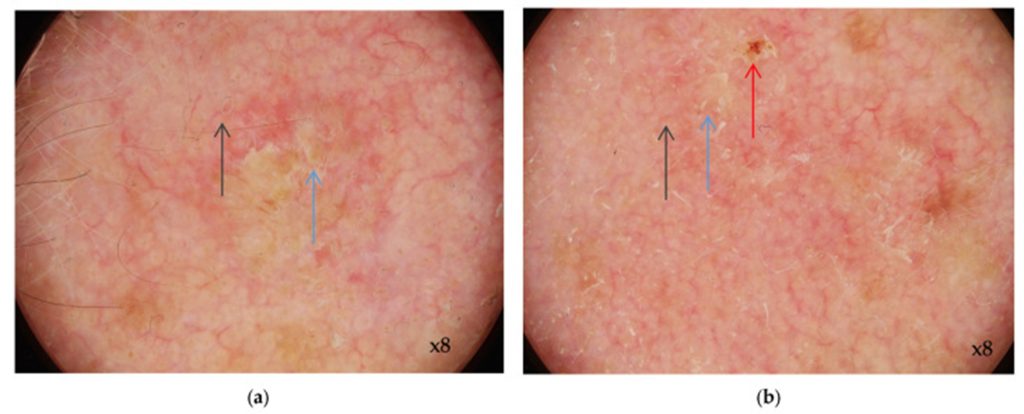
Figura 1. Dermatoscopia de la queratosis actínica
Seudorred roja con eritema de fondo interrumpido por las aberturas foliculares; escamas amarillas en la superficie (flechas azules); vasos ligeramente curvados y ondulados (flechas grises); erosión (flecha roja).
Creative Commons Attribution (CC BY) license: CC BY 4.0 DEED Attribution 4.0 International
El patrón de «explosión de estrella roja», con líneas dispuestas en un patrón radial o vasos en forma de horquilla que rodean un área de escamas de color amarillo a blanco son criterios que sugieren la transformación de QA en una lesión maligna.
La dermatoscopia aumenta la precisión para reconocer tumores cutáneos benignos y malignos, pero existen falsos positivos y negativos. Además, técnicas más nuevas, como la MCR, han demostrado alcanzar valores diagnósticos similares o incluso superiores.
Microscopía confocal de reflectancia
La MCR funciona como una modalidad intermedia entre la dermatoscopia y la histología tradicional, pues proporciona una visión lateral de las lesiones cutáneas y ofrece imágenes in vivo de la epidermis y las capas superiores de la dermis con una resolución cercana a la de las muestras histopatológicas. Asimismo, la MCR puede ser útil para evaluar el borde lateral de las lesiones para mejorar el resultado quirúrgico.
Sin embargo, su limitada capacidad de penetrar en profundidad en la piel (sobre todo en lesiones hiperqueratósicas, a menudo asociadas con CCE invasivo) obstaculiza la evaluación de la unión dermoepidérmica y la capa basal, ambas cruciales para el diagnóstico de patologías hiperqueratósicas potencialmente malignas. Puede ser preciso eliminar la hiperqueratosis antes de aplicar la MCR.
La distinción entre el CCE y la QA mediante MCR depende principalmente de la identificación de una atipia extensa de los queratinocitos en todo el espesor de la epidermis en el CCE, a diferencia de la QA, en la que la desorganización y la atipia ―si están presentes― suelen limitarse al estrato granuloso. En el CCE pueden observarse estructuras en forma de nido y células pleomórficas en la dermis, características que no están presentes en la QA.
Las características de QA observadas a través de MCR proporcionan una sensibilidad del 80 % y una especificidad del 98,6 % en la identificación de QA.
La QA se manifiesta típicamente con descamación superficial, paraqueratosis y un patrón en panal irregular en las capas espinogranulares. En la unión dermoepidérmica se observan a menudo pequeñas papilas dérmicas regulares (figura 2).
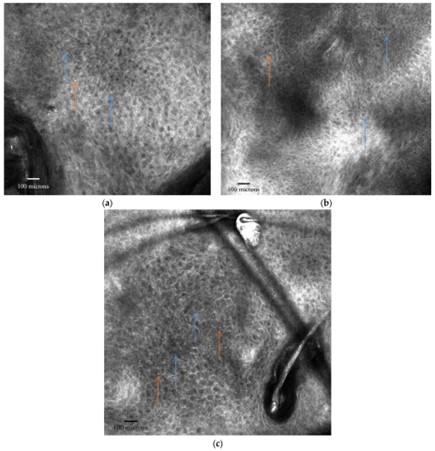
Figura 2. Microscopia confocal de reflectancia de la queratosis actínica
Patrones típicos de panal con queratinocitos de tamaño y morfología variables a nivel de las capas espinosa y granular (flechas azules); pequeñas células hiperreflectantes correspondientes a células inflamatorias (flechas naranjas).
Creative Commons Attribution (CC BY) license: CC BY 4.0 DEED Attribution 4.0 International
Estudios actuales muestran sensibilidades y especificidades que varían del 79–100 % y del 78–100 %, respectivamente, en el diagnóstico de QA, CCE in situ y CCE con MCR.
Tomografia de coherencia óptica
Ofrece imágenes no invasivas de la piel en tiempo real. Funciona de manera similar al ultrasonido, pero utiliza impulsos de luz cercanos a los infrarrojos y captura imágenes midiendo la intensidad de la luz reflejada a diferentes profundidades. Como puede penetrar hasta la unión dermoepidérmica, es particularmente efectiva para identificar QA. La TCO de alta definición (CTO-AD) es una variante de la TCO estándar con capacidades mejoradas, como la posibilidad de visualizar células cutáneas individuales y no solo estructuras y patrones más grandes.
Las características morfológicas de las QA en la TCO incluyen la alteración de las capas de la piel, la presencia de estrías y puntos blancos, hiperqueratosis y un aumento del grosor epidérmico.
En la CTO-AD, las QA se caracterizan por una estructura epidérmica desordenada y un patrón de panal atípico.
Ecografía e imágenes por ecografía de frecuencia alta
La ecografía de alta frecuencia ofrece ventajas significativas sobre la evaluación clínica, ya que proporciona información esencial para la detección y medición precisa de numerosas lesiones cutáneas clínicas y subclínicas.
La ecografía de alta frecuencia guiada por dermatoscopia integra la dermatoscopia con la ecografía de alta frecuencia para ofrecer de forma simultánea la imagen de la superficie de la piel y su profundidad completa.
A diferencia de la dermatoscopia, la MCR y la TCO ―que son costosos y tienen una profundidad de penetración limitada―, la ecografía de alta frecuencia tiene las ventajas de ser asequible, fácil de usar, repetible, en tiempo real, no invasiva y versátil. Proporciona imágenes detalladas de las capas de la piel y estructuras más profundas, lo que la convierte en una herramienta valiosa para el diagnóstico de tumores de piel sospechosos y para ayudar a tomar decisiones relacionadas con el tratamiento.
Campo de cancerización y papel de las técnicas de imagen no invasivas en el diagnóstico y seguimiento del tratamiento
Se han utilizado múltiples definiciones de campo de cancerización (CC). El Grupo de Trabajo de Progreso de Evidencia en QA (PEAK) lo define clínicamente como el «área anatómica con QA o adyacente a QA y piel visiblemente dañada por el sol identificada por al menos dos de los siguientes signos: telangiectasia, atrofia, trastornos de pigmentación y piel “de lija”». La simple identificación de un área de CC cambia el enfoque terapéutico, al asociarse técnicas de tratamiento del CC con métodos destructivos locales para las lesiones de QA.
Los métodos de imagen no invasivos permiten una fácil identificación del CC, a veces incluso en etapas precancerosas o incluso antes de la aparición de QA, y también suponen un método de seguimiento terapéutico eficiente y no invasivo.
La MCR permite identificar la desorganización queratinocítica antes de que sea visible dermatoscópicamente, lo cual permite iniciar el tratamiento en una fase temprana y aumentar así su eficacia. La MCR tiene una sensibilidad y una especificidad próximas a las histológicas.
Conclusiones
Las técnicas de imagen no invasivas permiten la identificación de criterios claros para establecer un diagnóstico de la QA y ofrecen al dermatólogo la oportunidad de seguir de cerca el CC, así como el tratamiento, con el objetivo de determinar cuándo finalizar el tratamiento.
En la actualidad, la MCR de reflectancia sigue siendo la técnica de imagen con la especificidad y sensibilidad más cercanas al examen histopatológico en el diagnóstico y seguimiento de estas lesiones.
ES-NOP-2400107