Psoriasis y microbiota intestinal: del eje intestino-piel a nuevas estrategias terapéuticas
Este artículo (Chen, et al. Psoriasis and gut microbes: research advances from mechanism to therapy) aborda tres temas relacionados con la psoriasis y la microbiota intestinal:
- Eje intestino-piel: tres mecanismos convergentes
- Modulación de la microbiota: estrategias terapéuticas emergentes
- Disbiosis intestinal en psoriasis: una conexión establecida
Eje intestino-piel: tres mecanismos convergentes
La disbiosis intestinal contribuye a la inflamación cutánea en psoriasis a través de tres mecanismos convergentes:
Desregulación inmunitaria. La microbiota alterada promueve un desequilibrio entre las células T reguladoras y las proinflamatorias (Th17) en el intestino, la misma vía que abordan los fármacos biológicos actuales. Las bacterias pro-inflamatorias activan la inmunidad innata intestinal, induciendo un exceso de citocinas clave (IL-17, TNF-α) que, por vía sistémica, alcanzan la piel y amplifican la hiperproliferación de queratinocitos.
Disfunción de la barrera intestinal. Los pacientes con psoriasis presentan un aumento de la permeabilidad intestinal («intestino permeable»), con marcadores de daño intestinal que se correlacionan directamente con la gravedad de la enfermedad (PASI). La barrera comprometida permite que endotoxinas bacterianas alcancen el torrente sanguíneo, activando la inflamación sistémica. Se ha detectado incluso ADN bacteriano circulante en estos pacientes, evidencia directa de la translocación intestinal.
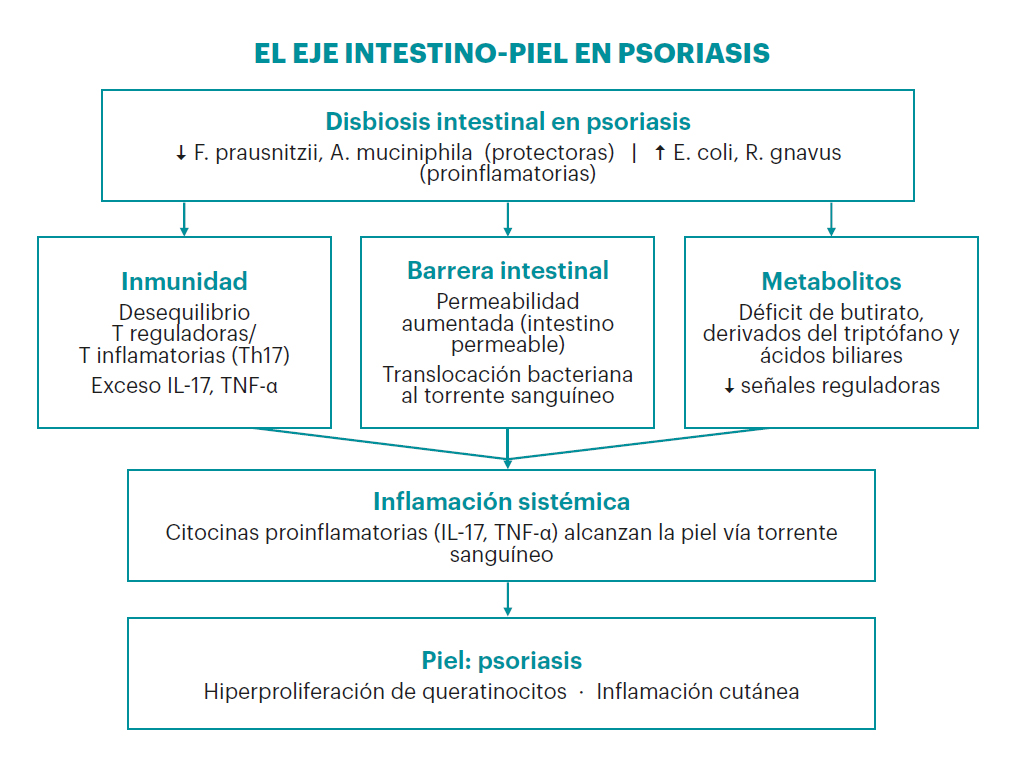
Figura 1. El eje intestino-piel en psoriasis
Fuente: Adaptada de Chen et al. (2025)
Metabolitos microbianos alterados. Tres familias median la comunicación intestino-piel y todas están reducidas en psoriasis: ácidos grasos de cadena corta (butirato), derivados del triptófano y ácidos biliares secundarios.
- Derivados del triptófano: los protectores disminuyen, en correlación directa con la gravedad.
- Ácidos biliares secundarios: reguladores del balance Treg/Th17, significativamente reducidos.
Mensajes clave
- La disbiosis intestinal altera la vía IL-23/Th17, la misma diana de los fármacos biológicos en psoriasis.
- La mayor permeabilidad intestinal permite la translocación de endotoxinas que activan la inflamación cutánea a distancia.
- El déficit de metabolitos protec-tores (butirato, indoles, ácidos biliares) priva al sistema inmunitario de señales reguladoras.
Modulación de la microbiota: estrategias terapéuticas emergentes
La evidencia sobre el papel de la disbiosis en psoriasis ha impulsado el estudio de intervenciones basadas en microbiota como posibles adyuvantes al tratamiento convencional.
Probióticos. Las cepas de Lactobacillus y Bifidobacterium son las más estudiadas. En ensayos clínicos aleatorizados (ECA), una mezcla de B. longum, B. lactis y L. rhamnosus mejoró las puntuaciones PASI, redujo marcadores inflamatorios sistémicos (PCR, TNF-α) y disminuyó el riesgo de recurrencia de la psoriasis. Los cambios en la flora intestinal se correlacionaron con la mejoría de la inflamación cutánea, reforzando el vínculo entre ambos sistemas.
Además, B. longum combinado con metotrexato potenció la eficacia del tratamiento convencional al preservar la barrera intestinal y mejorar el equilibrio inmunitario.
Prebióticos. La suplementación con FOS, XOS y GOS mejoró las puntuaciones PASI y DLQI frente a controles. La ingesta mantenida de GOS durante 10 semanas redujo significativamente las citocinas proinflamatorias y aumentó la IL-10 antiinflamatoria.
Simbióticos. La combinación de prebióticos (8 semanas) y probióticos (12 semanas) produjo reducciones significativas en marcadores inflamatorios, PASI y grosor de las lesiones frente a controles.
Trasplante de microbiota fecal (TMF). En modelos preclínicos, el TMF de donantes sanos restauró el equilibrio inmunitario y redujo la inflamación cutánea. Los primeros casos clínicos mostraron reducción de TNF-α sérico y mejoría del PASI, aunque un ECA en artritis psoriásica (n=31) no alcanzó significación estadística frente a placebo. La selección de donantes, la vía de administración y los protocolos de pretratamiento son áreas clave de investigación activa.
Tabla 1. Estrategias terapéuticas basadas en microbiota
| Estrategia | Evidencia destacada | Estado actual |
| Probióticos (Lactobacillus, Bifidobacterium) | ECA: mejoría PASI, 🠇marcadores inflamatorios, 🠇recurrencia |
ECA en humanos |
| Prebióticos (FOS, XOS, GOS) | Mejoría PASI y DLQI; 🠇citocinas proinflamatorias, 🠅IL-10 |
Ensayos clínicos |
| Simbióticos | Mejoría PASI, marcadores inflamatorios y grosor lesional |
Ensayos clínicos |
| Trasplante de microbiota fecal | Preclínico prometedor, casos clínicos positivos, ECA limitados |
Fase exploratoria |
Fuente: Adaptada de Chen et al. (2025)
Disbiosis intestinal en psoriasis: una conexión establecida
La microbiota intestinal ha dejado de ser un actor secundario en dermatología. En psoriasis, la evidencia acumulada sitúa el «eje intestino-piel» como un mecanismo patogénico relevante, con implicaciones tanto en la comprensión de la enfermedad como en nuevas estrategias terapéuticas. Los pacientes con psoriasis presentan, de hecho, un riesgo casi duplicado de colitis ulcerosa, lo que subraya la estrecha relación entre ambos sistemas.
Los hallazgos más consistentes incluyen:
- Menor diversidad microbiana: los principales índices de diversidad están significativamente reducidos en pacientes con psoriasis frente a controles sanos, indicando un ecosistema intestinal empobrecido.
- Desequilibrio Firmicutes/Bacteroidetes, los dos filos bacterianos dominantes en el intestino, reportado en la mayoría de estudios como marcador de disbiosis.
- Reducción de bacterias protectoras, especialmente Faecalibacterium prausnitzii (principal productora de butirato, un potente antiinflamatorio) y Akkermansia muciniphila (clave para la integridad de la barrera mucosa intestinal).
- Aumento de bacterias proinflamatorias como E. coli y R. gnavus, asociadas a respuestas inmunitarias aberrantes.
Mensajes clave
- Los pacientes con psoriasis presentan una disbiosis intestinal consistente: menor diversidad y desequilibrio en la composición.
- La reducción de F. prausnitzii y A. muciniphila compromete las defensas antiinflamatorias y la integridad de la barrera intestinal.
- La solapación genética y clínica entre psoriasis y enfermedad inflamatoria intestinal refuerza el papel patogénico del eje intestino-piel.
Referencia
Chen J, Sun K, Zhang X, Chen X, Chu Y, Geng L, Bian Z, Su Y, Cong X, Wang G. Psoriasis and gut microbes: research advances from mechanism to therapy. Front Microbiol. 2025;16:1711288. doi: 10.3389/fmicb.2025.1711288
ES-MTP-2600012